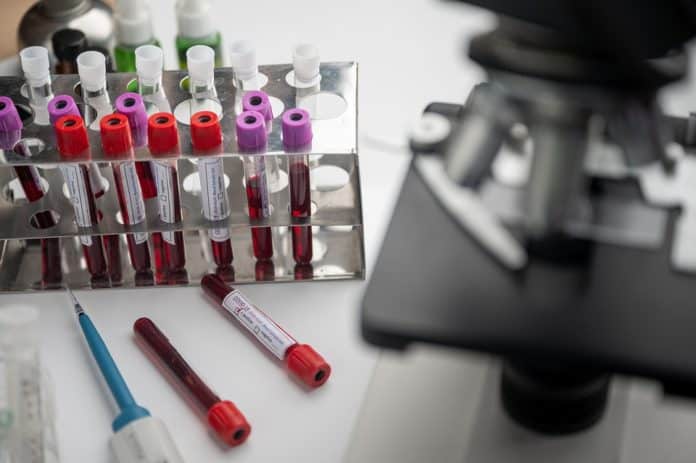
Um artigo publicado nesta segunda-feira (20) pela revista científica The Lancet concluiu que a vacina candidata da Universidade de Oxford, no Reino Unido, produzida em parceria com o laboratório AstraZeneca é promissora. O estudo, referente à Fase 1, demonstrou segurança, poucos efeitos secundários e estímulo à produção de anticorpos e células contra o novo coronavírus.
A vacina, que é considerada a mais avançada, começou a ter sua Fase 3 testada no Brasil na semana de 22 de junho. Além dos 2 mil voluntários em São Paulo, onde o ensaio é financiado pela Fundação Lemann, também participam voluntários no Rio de Janeiro, onde os testes são bancados pela Rede D’Or, e em Salvador. Todo o estudo no Brasil é liderado pela Unifesp (Universidade Estadual de São Paulo). No total, serão 5 mil voluntários no País.
Pesquisadores disseram que o imunizante de Oxford provocou efeitos colaterais brandos com mais frequência do que ocorre em um grupo de controle, mas que alguns destes puderam ser reduzidos com o uso de paracetamol e que ela não causou efeitos adversos graves.
Além do imunizante de Oxford, outras duas pesquisas anunciaram resultados promissores semelhantes nesta segunda-feira. A vacina contra a covid-19 desenvolvida pela CanSino Biologics Inc., em parceria com a unidade de pesquisa militar na China, apresentou resposta imune segura ao vírus.
A Biotech Ltd., empresa alemã de biotecnologia, em parceira com farmacêutica norte-americana Pfizer, também divulgaram hoje os dados adicionais de sua vacina experimental contra o coronavírus. Eles mostram que ela, assim como as outras duas, é segura e foi capaz de induzir resposta imunológica.
Porém, o imunizante testado pela universidade britânica é o estudo mais avançado e, por isso, a principal candidata no combate à pandemia, que já tirou mais de 600 mil vidas em todo o mundo.
“Esperamos que isto signifique que o sistema imunológico lembrará do vírus para que nossa vacina proteja as pessoas por um período prolongado”, disse o principal autor do estudo, Andrew Pollard, da Universidade de Oxford. “Entretanto, precisamos de mais pesquisas antes de podermos confirmar que a vacina protege efetivamente contra a infecção de SARS-CoV-2 (covid-19) e quanto tempo qualquer proteção dura.”
Após a divulgação dos dados, em coletiva de imprensa na sede da OMS (Organização Mundial da Saúde), em Genebra, o diretor do Programa de Emergências em Saúde da entidade, Mike Ryan, avaliou os dados de Oxford como “positivos”, mas ponderou que ainda há um longo caminho a ser percorrido até a viabilização de uma vacina.
A AstraZeneca assinou acordos com governos de todo o mundo para fornecer a vacina caso ela se mostre eficiente e obtenha aprovação regulatória. A empresa disse que não buscará lucrar com a vacina durante a pandemia. Um dos acordos foi feito com o governo brasileiro e prevê que a vacina seja produzida no País pela Fiocruz (Fundação Oswaldo Cruz).
Em junho, o Ministério da Saúde anunciou um acordo de cooperação para a compra e transferência de tecnologia para produção de vacinas contra a covid – 19 desenvolvidas pela Universidade de Oxford e pela AstraZeneca.
A previsão é de que o primeiro lote de vacinas, com 15,2 milhões de doses, chegue ao Brasil em dezembro, e mais 15,2 milhões em janeiro. O Brasil receberá o chamado IFA (ingrediente farmacêutico ativo), que será processado e envasado pela Fiocruz (Fundação Oswaldo Cruz).
Num segundo momento, com a transferência de tecnologia, a Fiocruz, por meio do instituto Bio-Manguinhos, também produzirá a vacina.
Como ainda não foi concluída a pesquisa clínica sobre a vacina, o governo explicou em nota que o acordo começa com uma encomenda “em que o Brasil assume também os riscos da pesquisa”.
A Unifesp divulgou na semana passada que a vacina britânica poderá ter o registro liberado em junho de 2021, exatamente um ano após o início dos testes no Brasil. Embora os estudos avancem em todo o planeta, o prazo de 12 a 18 meses para liberação é considerado um recorde. A vacina mais rápida já criada, a da caxumba, levou pelo menos quatro anos para ficar pronta.
O CRIE (Centro de Referência para Imunobiológicos Especiais) da Unifesp, que coordena a aplicação da vacina em São Paulo, informa que, até o momento, nenhum dos voluntários apresentou efeitos colaterais ou severos.
O Brasil também está testando a vacina produzida pelo laboratório chinês Sinovac Biotech, em uma iniciativa do Instituto Butantan. As primeiras doses do imunizante chegaram hoje ao País. O carregamento foi trazido por um voo de Frankfurt, na Alemanha, que aterrissou no Aeroporto Internacional de Guarulhos.
Segundo estudo publicado com revisão por partes na revista científica Science em maio, a vacina produzida pelo laboratório Sinovac, que começará Fase 3 de testes no Brasil, mostrou que os animais em teste que receberam doses maiores da vacina tiveram melhor resposta contra vírus. A primeira e a segunda fases dos testes clínicos contaram com centenas de voluntários na China.
Segundo o G1, as vacinas devem chegar ao Butantan ainda nesta segunda-feira. Na primeira etapa de testes, já autorizada pela Anvisa (Agência Nacional de Vigilância Sanitária), serão vacinados profissionais de saúde de São Paulo, Rio Grande do Sul, Minas Gerais e Paraná, além do Distrito Federal.
Nas últimas 24 horas o Brasil registrou 753 novas mortes e 23.265 novos infectados pelo novo coronavírus. Os dados são do Conass (Conselho Nacional dos Secretários de Saúde) e foram divulgados às 18h deste domingo. No total, o País tem 79.488 mortes e 2.098.389 casos de covid-19.
Outra potencial vacina contra a covid-19 está sendo desenvolvida na China pela empresa CanSino Biologics e pelo Instituto de Biotecnologia e a Academia de Ciências Médicas Militares do país asiático. Ela mostrou-se segura e induziu resposta imunológica na maioria dos pacientes que a receberam, disseram pesquisadores em estudo científico.
A candidata a vacina da CanSino, chamada de Ad5-nCOV, é uma das várias que mostraram-se promissoras em testes em humanos e que estão caminhando para o estágio final de testes, ao lado de potenciais vacinas da Moderna Inc, Sinovac Biotech Ltd. e Inovio Pharmaceuticals Inc, que ainda não tiveram o resultados avançados divulgados pelos cientistas.
Embora a vacina da CanSino ainda tenha de iniciar os testes em estágio avançado em larga escala para avaliar quão bem ela previne que as pessoas sejam infectadas, já recebeu aval para ser usada em militares chineses – por isso, é a que está em fase mais avançada no país asiático. Os resultados dos estudos de etapa intermediária, publicados pela revista médica The Lancet, dão suporte para a vacina ser testada em um estudo mais amplo.
A candidata a vacina usa um adenovírus para carregar material genético da proteína do novo coronavírus para o corpo humano, um método também usado pelos pesquisadores da Universidade de Oxford.
As respostas imunes provocadas pela vacina podem ser minadas se a pessoa que a recebeu já tiver desenvolvido uma alta imunidade a adenovírus por causa de uma infecção anterior, disseram os pesquisadores chineses.
De acordo com dados da Refinitiv, a CanSino tem como sua principal acionista a Lilly Asia Ventures, apoiada pela gigante farmacêutica norte-americana Eli Lilly.
Já a empresa alemã BioNTech e a farmacêutica norte-americana Pfizer Inc. disseram que os dados de um estudo em estágio inicial de sua vacina contra o coronavírus mostraram que ela provocou resposta imune e foi bem tolerada, semelhante aos resultados observados em testes anteriores.
Estudo foi realizado na Alemanha com 60 voluntários saudáveis; a vacina induziu anticorpos neutralizantes de vírus naquelas que receberam duas doses, de acordo com os resultados anteriores de estudo nos EUA em estágio inicial.
No estudo alemão, a vacina também gerou um alto nível de respostas das “células T” contra o coronavírus. As células T, um tipo de glóbulo branco, são um componente importante do ataque do sistema imunológico contra invasores estrangeiros, como vírus.
“Os dados de hoje incluem a primeira evidência de que a vacina gera uma resposta de células T, o que pode ser crítico para que os pacientes desenvolvam imunidade durável ao novo coronavírus”, disse o analista do Mizuho, Vamil Divan.
Os voluntários do estudo não apresentaram efeitos colaterais graves da vacina, embora alguns tenham relatado sintomas semelhantes aos da gripe e reações no local da injeção.
By Equipe HuffPostReuters